氯化钠
晶体结构
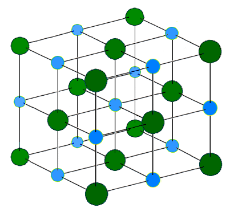
NaCl晶体结构图。每个离子有六个相邻的离子,组成一个八面体。这种结构叫做 立方最密堆积 ( ccp )。
氯化钠的晶体形成立体对称。
其晶体结构中,较大的氯离子排成立方最密堆积,较小的钠离子则填充氯离子之间的八面体的空隙。每个离子周围都被六个其他的离子包围着。
这种结构也存在于其他很多化合物中,称为氯化钠型结构。
性质
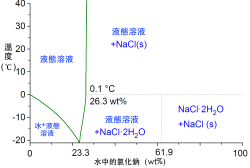
常压下水盐体系的相图
氯化钠是一种离子化合物,化学式为 NaCl {\displaystyle {\ce {NaCl}}} ,代表钠离子与氯离子的比例是一比一。海盐及新鲜开采的石盐(多数来自史前海洋)也含有微量的稀有元素,这些稀有元素通常对动植物的健康有益。氯化钠结晶是半透明的立方体,在正常情况下是白色的,但也可能会因杂质而呈现出蓝或紫的色调。氯化钠的摩尔质量是58.443克/摩尔,熔点为801 °C(1,474 °F),沸点为1,465 °C(2,669 °F),密度是每立方厘米2.17克。氯化钠易溶于水,常温下在水中的溶解度是359克/升,溶于水时完全电离为钠离子与氯离子 。从冷溶液中析出的盐当中,每个盐分子带有两个结晶水:NaCl·2H 2 O。食盐水的物理性质与纯水有较大的差异。常压下,水盐体系的低共熔点为−21.12 °C(−6.02 °F),低共熔物中盐的质量分数为23.31% 。该质量分数的食盐水沸点约为108.7 °C (227.7 °F) 。
生物意义
氯化钠对于地球上的生命非常重要。
大部分生物组织中含有多种盐类。血液中的钠离子浓度直接关系到体液的安全水平的调节。
由信号转换导致的神经冲动的传导也是由钠离子调节的。
含氯化钠0.9%的水称为生理盐水,因为它与血浆有相同的渗透压。生理盐水是主要的体液替代物,广泛用于治疗及预防脱水,也用于静脉注射治疗及预防血量减少性休克。
人类与其他灵长类不同,人类通过出汗分泌大量的氯化钠。
来源
海水和盐湖是氯化钠的主要来源,海水中含氯化钠还存在于盐湖的沉积物中,如中国的班戈等湖区。
制法
蒸发咸水(如晾晒海水),在水没有完全蒸干前滤出氯化钠晶体。适合大量生产。
少量精制:将粗盐溶解于水中,过滤掉不溶性杂质,再加精制剂如NaOH、Na 2 CO 3和CaCl 2等,使SO 4 2−、Ca 2+、Mg 2+等可溶性杂质转化成沉淀,并滤除。最后用盐酸将pH调节至7以下,蒸干溶液,得到氯化钠晶体。
实验室里的制备方法:将过量的盐酸和氢氧化钠溶液混合,蒸干溶液,析出氯化钠晶体 。
工业用途
根据1974年的统计数据,美国生产的食盐中只有2.7%作为家用食盐出售,16.6%用于路面除冰,4.2%用于动物饲料,1.8%用于硬水软化,剩余60%以上均被用于工业生产。食盐是无机重化工业的基础,在无机化工中,使用的食盐比其他任何原料都要多。其中,消耗食盐最多的工艺是氯碱法,该工艺通过电解食盐水制备氢氧化钠、氯气和氢气,通过电解熔盐获得金属钠和氯气。氯气主要被用于合成含氯有机化合物(如氯氟烃、聚氯乙烯)和消毒漂白,氢氧化钠则被广泛运用于无机化工和纸浆处理。另一种消耗食盐量比较大的工艺是氨碱法,该法通过往食盐水中注入氨和二氧化碳来制备碳酸氢钠,进而制备碳酸钠。大部分碳酸钠被用于制造玻璃。
氯碱工业中,电解氯化钠水溶液,产生氢气、氯气和氢氧化钠。
电解熔融氯化钠制备金属钠。可加入助熔剂(如氯化钙)降低熔点。
氨碱法、联合制碱法中,氯化钠和二氧化碳、氨气一起制备纯碱。
注释
^ 低共熔点是盐水能够达到的最低温度。质量分数大于23.31%的盐水在冷却到该温度之前会析出盐(或其水合物),质量分数小于23.31%的盐水在冷却到该温度之前则会析出冰。
参考资料
免责声明:以上内容版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。感谢每一位辛勤著写的作者,感谢每一位的分享。

- 有价值
- 一般般
- 没价值








24小时热门
推荐阅读
关于我们

APP下载



























{{item.time}} {{item.replyListShow ? '收起' : '展开'}}评论 {{curReplyId == item.id ? '取消回复' : '回复'}}